Einleitung
Für die erfolgreiche Anwendung von Biosensoren in vivo und aktiven Mikroimplantaten in der medizinischen Diagnostik und Therapie ist die Ankopplung des biologischen Gewebes an die technische Oberfläche wesentlich für die Funktion der Implantate. Die Untersuchung der erforderlichen Stabilität der verwendeten Materialen sowie der durch den Werkstoff bedingten biologischen Reaktionen des Gewebes und der Auswirkung gezielter chemischer Modifikationen der technischen Oberfläche sind daher von entscheidender Bedeutung. Ein zentraler Punkt ist dabei die morphologische Analyse der Grenzfläche zwischen Werkstoff und Zellen beziehungsweise biologischem Gewebe bei hoher lateraler Auflösung.
Am Beispiel eines subretinalen elektronischen Sehimplantats, das bei krankheitsbedingter Degeneration der Photorezeptoren und daraus resultierender Erblindung als Sehprothese für die elektrische Stimulation retinalen Gewebes entwickelt wurde [1], wird eine Präparations- und Analysemethode für die Untersuchung der entsprechenden biologisch-technischen Grenzfläche vorgestellt. Sie basiert auf der Kombination von klassischer biologischer Präparation für die Elektronenmikroskopie und ausgewählter Dünn- beziehungsweise Querschlifftechnik, die üblicherweise im materialwissenschaftlichen Bereich zum Einsatz kommt. Zusammen mit der lokal sehr präzisen Zielpräparation in einem Crossbeam®-Elektronenionenmikroskop ergibt sich so eine Präparations- und Analysemethode, die eine hochaufgelöste strukturelle Untersuchung der biologisch-technischen Grenzfläche ermöglicht.
Das subretinale Sehimplantat
Das Konzept des subretinalen Sehimplantats beruht auf dem Ansatz, dass bei einer Erblindung durch Retinitis Pigmentosa trotz krankheitsbedingter Degeneration der Photorezeptoren der Großteil des retinalen Nervengewebes unverändert erhalten bleibt und somit für die Signalweiterleitung und Signalverarbeitung weiterhin genutzt werden kann. Werden die degenerierten Photorezeptoren durch ein geeignetes intelligentes Implantat ersetzt, welches zwischen Netzhaut und Aderhaut liegt und mittels lichtabhängiger elektrischer Stimuli Reize erzeugt, kann daher ein Seheindruck erzeugt werden (Abb. 1).

Abb. 1: (a) Schematische Übersicht zur Funktionsweise des subretinalen Sehimplantats: Ein geeignetes intelligentes Implantat ersetzt die krankheitsbedingt degenerierten Photorezeptoren; der Seheindruck wird mittels lichtabhängiger elektrischer Stimuli erzeugt, wobei der unveränderte Teil des retinalen Nervengewebes weiterhin für die Signalweiterleitung und Signalverarbeitung genutzt wirdQuelle: www.retinaimplant.de [2]; (b) Fundus-Aufnahme eines Sehimplantats am Augenhintergrund
Der Aufbau des subretinalen Sehimplantats besteht im Wesentlichen aus einem etwa 3 x 3 mm2 großen Siliziumchip mit insgesamt 1500 Pixel. Jeder Pixel besteht aus einer lichtempfindlichen Photodiode, einem Verstärker und einer Stimulationselektrode zur Übertragung des elektrischen Reizes an das retinale Gewebe. Um die elektrische Versorgung des Chips zu gewährleisten, ist der Chip auf einer flexiblen, mit Leitbahnen versehenen Polyimidfolie befestigt, die in ein dünnes Kabel übergeht. Die benötigte Energie für das System wird, ähnlich dem Cochlea Implantat, hinter dem Ohr induktiv von außen eingekoppelt (Abb. 2). Für die Effizienz der Übertragung des Reizsignals vom Chip auf die Netzhaut ist es wichtig, dass die Netzhaut nach Implantation flächig am Chip anliegt und die Stimulationselektroden in direktem Kontakt mit den äußeren Zellschichten der Netzhaut stehen.

Abb. 2: Übersicht über den technischen Aufbau des subretinalen Sehimplantats bestehend aus dem Siliziumchip mit 1500 Pixeln mit einer Photodiode, einem Verstärker und einer Stimulationselektrode pro Pixel; der Siliziumchip ist zur elektrischen Versorgung auf einer mit Leitbahnen versehenen flexiblen Folie befestigt, die über ein Kabel mit der induktiven Energieversorgung verbunden ist
Quelle: www.retinaimplant.de [2]
Präparation der biologisch-technischen Grenzfläche für die Elektronenmikroskopie
Für die morphologische Untersuchung des Kontakts zwischen Elektrode und Netzhaut im Elektronenmikroskop wird ein Netzhautpräparat einer Ratte in vitro auf einen einzelnen Chip aufgebracht und mittels gepufferter Glutaraldehydlösung fixiert. Nach der Fixierung wird das biologische Gewebe mit Schwermetallen (Uranylacetat und Osmiumtetroxid) kontrastiert. Die Schwermetalle binden dabei unterschiedlich stark an Membranen und Lipide und können dadurch die innere Zellstruktur im Elektronenmikroskop sichtbar machen. Nach der Kontrastierung wird das Gewebe mittels Alkohol entwässert und in Epoxidharz eingebettet, um eine für die Anforderungen des Elektronenmikroskops geeignete Probe zu erhalten. Durch die Auspolymerisation des Epoxidharzes im Ofen bekommt man für die weiteren Präparationsschritte einen kompakten Probenblock aus Epoxidharz (Abb. 3).

Abb. 3: Schematische Darstellung des Protokolls zur Präparation biologischer Proben für die Elektronenmikroskopie; nach der Einbettung in Epoxidharz erhält man, schematisch gezeigt, einen kompakten Probenblock mit dem heterogenen Probensystem Sehimplantat und retinales Gewebe
Präparation eines Dünnschliffs für die Analyse in einem Crossbeam®-Elektronenionenmikroskop
Bei konventionellen biologischen Proben werden von entsprechenden Probenblöcken aus üblicherweise elektronenmikroskopische Dünnschnitte mit einem Ultramikrotom angefertigt und auf geeignete Halter aufgebracht, um mit einem Transmissionselektronenmikroskop (TEM, transmission electron microscope) oder mit einem niederenergetischen Rasterelektronenmikroskop (SEM, scanning electron microscope) abgebildet zu werden. Diese Präparationsmethode ist allerdings auf weiche, homogene Proben beschränkt. Ein heterogenes Probensystem aus hartem und weichem Material, wie es im Fall des subretinalen Sehimplantates aus Silizium in Kombination mit dem weichen, retinalen Gewebe vorliegt, kann mittels eines Ultramikrotoms nicht artefaktfrei geschnitten werden.
Daher soll das vorliegende Probensystem aus Sehimplantat und retinalem Gewebe mit einem Crossbeam®-Elektronenionenmikroskop (Zeiss Auriga 40), also einem kombinierten Zweistrahlgerät, welches mit einer Gallium-Ionensonde (FIB, focused ion beam) und einem niederenergetischen Rasterelektronenmikroskop (SEM) ausgestattet ist, untersucht werden. Zweistrahlgeräte (FIB-SEM) ermöglichen mit der Gallium-Ionensonde die zielgenaue Präparation von Mikroquerschnitten senkrecht zur Probenoberfläche. Diese Mikroquerschnitte können dann mit dem niederenergetischen Rasterelektronenmikroskop bei hoher lateraler Auflösung abgebildet werden (Abb. 4).

Abb. 4: a) Schematische Darstellung des Aufbaus und der Funktionsweise eines Crossbeam®-Elektronenionenmikroskops bestehend aus der Kombination einer fokussierten Ionensonde (FIB) und eines niederenergetischen Rasterelektronenmikroskops (SEM); das FIB erzeugt in lokaler Zielpräparation einen Mikroquerschnitt in der Probe, der von dem SEM abgebildet wird. b) Beispiel einer FIB-SEM-Analyse an einem retinalen Chip ohne Gewebe: 1) rasterelektronenmikroskopische Aufnahme der Oberfläche eines retinalen Chips mit neun Mikroelektroden, 2) der FIB-Mikroquerschnitt durch eine der Mikroelektroden zeigt den Aufbau des Chips mit den verschiedenen Leitbahnebenen, 3) an dem Mikroquerschnitt werden mittels energiedispersiver Röntgenanalyse (EDX, energy disperive X-ray spectroscopy) die Elemente innerhalb des Schichtaufbaus bestimmt
Voraussetzung für die Präparation solcher Mikroquerschnitte sowie deren Analyse in einem FIB-SEM-Instrument ist allerdings, dass die interessierenden Strukturen nur wenige 10 µm von der Probenoberfläche entfernt in der Tiefe der Probe liegen. Bei dem vorliegenden Probensystem besteht daher noch die Schwierigkeit in der Position der biologisch-technischen Grenzfläche innerhalb des Epoxid-Probenblocks. Die Grenzfläche liegt im Beispiel des Sehimplantats mit retinalem Gewebe einige hundert Mikrometer bis einige Millimeter innerhalb der Probe. Die Dicke des Chips einerseits und die Dicke des retinalen Gewebes auf der anderen Seite erschweren den Zugang zur Grenzfläche deutlich. Außerdem liegt die biologisch-technische Grenzfläche im Allgemeinen nicht parallel zu einer der Probenblockseiten vor (Abb. 5).

Abb. 5: (a) Schematische Übersicht über das Probensystem, das aus retinalem Gewebe und subretinalem Sehimplantat besteht und in Epoxidharz eingebettet ist; (b) durch Schleifen und Polieren wird eine Probe hergestellt, die parallel zur biologisch-technischen Grenzfläche dünngeschliffen und lichtmikroskopisch transparent ist; (c) im schematischen Querschnitt ist deutlich die Verringerung der Probendicke auf 10 µm bis 50 µm zu sehen sowie die biologisch-technische Grenzfläche, die durch das Dünnschleifen der FIB-SEM-Analyse zugänglich gemacht wird
Daher kommen ausgewählte mechanische Präparationsmethoden wie Schleifen und Polieren, die konventionell im materialwissenschaftlichen Bereich eingesetzt werden, für die weitere Probenpräparation zum Einsatz. Durch die Verwendung dieser mechanischen Präparationsmethoden kann unter Einsatz geeigneter Schleif- und Poliermittel ein Dünnschliff erzeugt werden, der parallel zur biologisch-technischen Grenzfläche ausgerichtet ist. Dieser Dünnschliff ermöglicht FIB-SEM-Analysen über einen weiten Bereich der Grenzfläche. Darüber hinaus kann durch diese Präparationsmethode die biologisch-technische Grenzfläche auch mittels lichtmikroskopischer Methoden analysiert werden. Dadurch ist es möglich lichtmikroskopische Durchlicht- und Auflichtbilder mit Aufnahmen der Probenoberfläche, die man mittels der niederenergetischen Rasterelektronenmikroskopie erhält, zu korrelieren. Die resultierenden Aufnahmen helfen dabei, den für die folgende FIB-SEM-Analyse interessanten Bereich festzulegen (Abb. 6).

Abb. 6: Links: Lichtmikroskopische Übersicht über den Dünnschliff mit retinalem Gewebe (braun gefärbt aufgrund der Schwermetallkontrastierung) und den Mikroelektroden des Chips; Mitte: rasterelektronenmikroskopische Übersicht über die Oberfläche des Dünnschliffs in Korrelation zu den lichtmikroskopischen Aufnahmen sowie mit zwei FIB-SEM-Mikroquerschnitten; rechts: FIB-SEM-Mikroquerschnitt durch eine Stimulationselektrode mit dem Chip mit Verkapselungsmaterial und dem retinalen Gewebe
FIB-SEM-Analyse und 3D-Tomographie der biologisch-technischen Grenzfläche
Für die FIB-SEM-Analyse wird eine einzelne Stimulationselektrode mit dem umgebenden retinalen Gewebe mittels lichtmikroskopischer Aufnahmen als interessanter Bereich (ROI, region of interest) festgelegt. Unter Verwendung eines Crossbeam®-Elektronenionenmikroskops wird dann an dieser Stimulationselektrode eine FIB-SEM-Serienschnitt-Tomographie [3] durchgeführt. Hierbei wird mit der fokussierten Ionensonde eine Serie von Mikroquerschnitten präpariert, welche jeweils die biologisch-technische Grenzfläche enthalten. Jeder dieser Mikroquerschnitte wird mit dem niederenergetischen Rasterelektronemikroskop abgebildet.
Für die Akquise der Bilder wird der Detektor für Energie selektierte Rückstreuelektronen (EsB-Detektor, Energy selected Backscatter detecor) verwendet, der bei Schwermetall kontrastierten biologischen Proben aufgrund des Materialkontrasts einen außergewöhnlich hohen Kontrast liefert. Außerdem zeigen die Bilder bei Verwendung dieses Detektors keine gegebenenfalls durch das FIB induzierten Schneidartefakte, da Aufnahmen unter Verwendung rückgestreuter Elektronen de facto keine topographische Information enthalten.
Mit typischen Voxelgrößen im Bereich von 10 x 10 x 10 nm für jede Raumrichtung kann man so morphologische Informationen bei hoher lateraler Auflösung in dem gesamten interessierenden Volumen der biologisch-technischen Grenzfläche erhalten (Abb. 7).

Abb. 7: Schematische Darstellung der Aufnahme eines FIB-SEM-Serienschnitt-Tomogramms an einer einzelnen Stimulationselektrode: Übersicht über das Kammerinnere des Crossbeam®-Instruments mit der Probe, Ionensonde und Rasterelektronenmikroskop; in den resultierenden Mikroquerschnitten sind der Siliziumchip mit Verkapselung und Stimulationselektrode im oberen Bereich der Mikroquerschnitte sowie darunter das retinale Gewebe deutlich zu erkennen, typische Voxelgrößen sind 10 x 10 x 10 nm
3D-Rekonstruktion der biologisch-technischen Grenzfläche
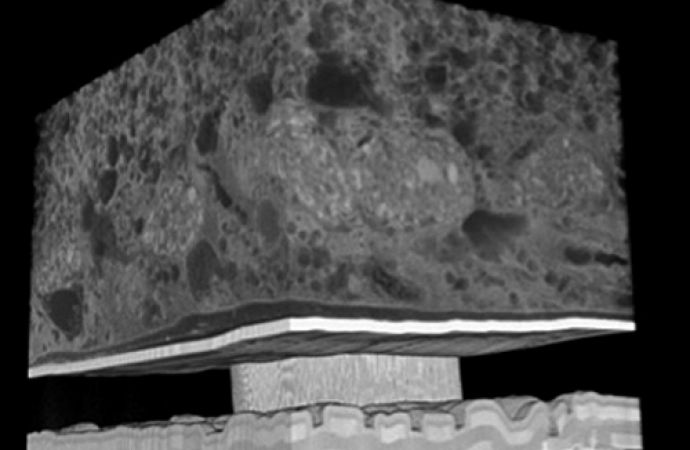
Der aus der FIB-SEM-Serienschnitt-Tomographie resultierende Stapel von zweidimensionalen Bildern ermöglicht mittels geeigneter Bildverarbeitungssoftware dreidimensionale Rekonstruktionen des analysierten Volumens. Für die Bildbearbeitung und die 3D-Rekonstruktion wird die Software ImageJ [4], ausgerüstet mit den Plugins StackReg [5], VolumeJ [6] und 3D Viewer [7], verwendet. Damit können die notwendigen Ausrichtungen der einzelnen Bilder zueinander durchgeführt sowie verschiedene dreidimensionale Darstellungen erzeugt werden (Abb. 8). Die resultierenden 3D-Rekonstruktionen helfen bei der Analyse der morphologischen Aspekte der biologisch-technischen Grenzfläche, wie zum Beispiel dem Abstand des retinalen Gewebes von der Mikroelektrode (Abb. 9). Im vorgestellten Beispiel zeigen die Bilder einen flächigen, direkten Kontakt der Stimulationselektroden mit dem Netzhautpräparat, so dass eine optimale Einkopplung des Stimulationssignals in die Netzhaut gewährleistet ist.

Abb. 8: Dreidimensionale Rekonstruktion der Stimulationselektrode auf dem Chip mit retinalem Gewebe nach der Bildbearbeitung mit ImageJ und unter Verwendung des Plugins 3D Viewer [7]; der Kontrast wurde so angepasst, dass das Verkapselungsmaterial transparent erscheint

Abb. 9: Vier Schnitte mit beliebiger Orientierung durch das rekonstruierte dreidimensionale Volumen unter Verwendung der Software ImageJ und des Plugins VolumeViewer [8], mit retinalem Gewebe in engem Kontakt zu der Mikroelektrode des Siliziumchips und detaillierter Struktur des retinalen Gewebes sowie den Details des CMOS-Elektronik
Zusammenfassung
Die Kombination von klassischen biologischen und ausgewählten mechanischen Präparationsmethoden mit der 3D-FIB-SEM-Serienschnitt-Tomographie ermöglicht eine Nanoanalyse komplexer heterogener Probensysteme, die sowohl aus weichem biologischem Material als auch aus hartem Material bestehen. Die dreidimensionale Rekonstruktion der biologisch-technischen Grenzfläche ermöglicht Aussagen zur Funktion von Implantaten, die auf einem engen Kontakt zwischen den für Sensoren und Aktoren verwendeten Materialien und dem umgebenden Gewebe beruht.
Kontakt
*NMI Naturwissenschaftliches und Medizinisches Institut an der Universität Tübingen, Markwiesenstraße 55, D-72770 Reutlingen
birgit.schroeppel@nmi.de
Literatur
[1] E. Zrenner et al.; Proc. R. Soc. B, 278 (1711), 2011, S. 1489–1497
[2] www.retina-implant.de
[3] L. Holzer et al.; J. Am. Ceram. Soc. 89, 2006, S. 2577–2585
[4] M. D. Abramoff et al.; Biophotonics International, 11, 2004, S. 36–42
[5] P. Thevenaz et al.; IEEE Trans Image Process, 7, 1998, S. 27–41
[6] M. D. Abramoff et al.; IEEE Trans Med. Imag., 21, 2002, S. 269–272
[7] B. Schmidt et al.; BMC Bioinformatics, 11, 2010, S. 274
[8] K. U. Barthel, Volume Viewer, [http://rsb.info.nih.gov/ij/plugins/volume-viewer.html]
DOI: 10.7395/2013/Schroeppel1
Für die erfolgreiche Anwendung von Biosensoren in vivo und aktiven Mikroimplantaten in der medizinischen Diagnostik und Therapie sind die Ankopplung des biologischen Systems an die technische Oberfläche sowie die Stabilität der verwendeten Biomaterialien von entscheidender Bedeutung für die Funktion des Implantats. Ein wichtiger Punkt ist dabei die morphologische Analyse der biologisch-technischen Grenzfläche bei hoher räumlicher Auflösung. Am Beispiel eines subretinalen elektronischen Sehimplantats, das für die elektrische Stimulation retinalen Gewebes bei bestimmten degenerativen Erkrankungen der Retina entwickelt wurde, wird eine für biologisch-technische Grenzflächen geeignete Präparations- und Analysemethode vorgestellt. Hierbei werden klassische biologische Präparationsmethoden (Fixierung, Kontrastierung, Einbettung in Epoxid-Harz) und konventionelle Dünn- bzw. Querschlifftechniken mit der Zielpräparation von Mikroquerschnitten, die in einem CrossBeam Elektronenionenmikroskop mittels fokussiertem Gallium-Ionenstrahl (FIB Focused Ion Beam) und niederenergetischem Rasterelektronenmikroskop (SEM Scanning Electron Microscope) möglich ist, kombiniert. Ausgehend von einzelnen mittels FIB und SEM erzeugten Abbildungen des Mikroquerschnittes der biologisch-technischen Grenzfläche können Serien von Abbildungen als tomographischer Datensatz aufgenommen werden, um eine dreidimensionale Rekonstruktion der Grenzfläche zu erhalten. Dies ermöglicht die morphologische Analyse der Grenzfläche zwischen biologischen und technischen Systemen bei hoher räumlicher Auflösung.
Electron Microscopy as an Analytical Tool for the Study of Implant Surfaces and the Interface
between Biological Matter and Technological Devices
For successful application of biosensors in vivo and active micro implants in medical diagnostics and therapy, coupling and connection of the biological system to the technical surface as well as stability of the biomaterials used is of crucial relevance for the performance of the implant. Thereby, an important point is the morphological analysis of the biological technical interface with high spatial resolution. On the example of a subretinal electronic implant developed for the electrical stimulation of retinal tissue in case of specific degenerative diseases of the retina, a preparation and analysis method suitable for biological technical interfaces will be presented. Therefore, conventional biological preparation methods for tissue based samples (fixation, staining, embedding in epoxy resin) and conventional thin section and cross section grinding and polishing methods are combined with the micro cross section preparation method which is given by a Crossbeam electron ion microscope using FIB technology and low voltage scanning electron microscopy (SEM). Starting with individual images of micro cross sections of the biological technical interface acquired with FIB and SEM tomographic data sets of the interface can be recorded by taking a series of micro cross section images to achieve a 3D reconstruction of the interface. This allows morphological analysis of the interface between biological and technical systems with high spatial resolution.