CVD-Synthese von Kohlenstoff-Nanoröhren zur Nutzung als Mikroelektroden für neuronale Anwendungen
In der Forschung werden häufig Mikroelektroden-Arrays (MEAs) für Experimente mit Zellkulturen eingesetzt. Neben dem etablierten Elektrodenmaterial Titannitrid kommen auch kohlenstoffbasierte Materialen wie beispielsweise Kohlenstoffnanoröhren in Frage, von denen man sich verbesserte Elektrodeneigenschaften verspricht. Die Synthese und Charakterisierung von Kohlenstoffnanoröhren-Elektroden auf MEAs wird im folgenden Artikel näher beschrieben.
CVD-Synthesis of Carbon Nanotubes for Use for Micro Electrodes
Micro electrode arrays (MEAs) are often deployed in research for experiments with cell cultures. Besides the established electrode material titanium nitride, carbon based materials like carbon nanotubes come into consideration, which are deemed to have enhanced electrode properties. The synthesis and characterisation of carbon nanotube electrodes on MEAs is described in the following article.
Einleitung
MEAs (Abb. 1), sind in der Forschung etablierte Mikrosysteme zur Detektion und Stimulation elektrischer Aktivität von Zellen in Zell- und Gewebekulturen [1]. Anwendung finden sie beispielsweise in der Grundlagenforschung bei der Untersuchung der Dynamik und Plastizität von neuronalen Netzwerken oder in der angewandten Forschung bei der Untersuchung der Wirkung pharmazeutischer Wirkstoffe auf die Aktivität von Herzmuskel- und Nervenzellen in Zellkultur. MEAs enthalten bis zu 256 Mikroelektroden (Durchmesser zwischen 10 µm und 100 µm), die über isolierte Zuleitungen kontaktiert werden können. Die Mikroelektroden können sowohl für die Messung zellulärer Signale als auch zur elektrischen Stimulation verwendet werden. Hierzu müssen sie – im Kontakt mit dem Kulturmedium im Zellkulturgefäß – eine möglichst hohe Grenzflächenkapazität aufweisen. Dies ist die Voraussetzung für eine geringe Impedanz und damit für ein hohes Signal-Rausch-Verhältnis bei der Messung und für eine hohe Ladungsübertragungskapazität für eine effiziente elektrische Stimulation.

Abb. 1: Mikroelektroden-Array für elektrophysiologische Untersuchungen an Zellkulturen. Das Elektrodenfeld im Zentrum eines Kulturgefäßes ist über Leiterbahnen mit den außenliegenden Kontaktpads verbunden
Als besonders geeignet zur Herstellung von multifunktionalen Elektroden gelten Kohlenstoff-Nanoröhren (CNTs, Carbon Nanotubes), da sie aufgrund ihrer besonderen Struktur große Grenzflächen ausbilden und besondere elektrochemische Eigenschaften haben.
Grundlagen zu CNTs
CNTs sind eine Modifikation des Kohlenstoffs, welche in CVD- (Chemical Vapor Deposition) Verfahren substratbasiert und gleichzeitig strukturiert synthetisiert werden können. Charakteristisch für CNTs sind die dem Graphit entsprechende Wandstruktur der zylindrischen Röhren, das heißt hexagonale Anordnung der Kohlenstoffatome, ein Durchmesser von bis zu 100 nm und Längen typischerweise im µm-Bereich. Mehrwandige CNTs sind typischerweise metallisch und zeichnen sich durch ihre sehr hohe Stromleitfähigkeit sowie ihre hohe mechanische Stabilität aus. Voraussetzung zur CNT-Synthese ist das Vorhandensein einer dünnen Schicht aus einer der katalytisch wirkenden ferromagnetischen Metalle Nickel, Kobalt oder Eisen.
Anforderungen an MEAs
Neben der notwendigen Biokompatibilität und -stabilität sowohl der Mikroelektroden als auch der restlichen MEA-Oberfläche sind eine möglichst geringe Impedanz und eine möglichst hohe Ladungsübertragungskapazität wünschenswerte Merkmale eines MEAs. Geringe Impedanzen gehen einher mit einem kleinen Grenzflächenrauschen und damit mit einem hohen Signal-Rausch-Verhältnis. Eine hohe Ladungsübertragungskapazität ermöglicht eine effiziente elektrische Stimulation mit kleiner Spannung, was zur Vermeidung unerwünschter, irreversibler Grenzflächenreaktionen wünschenswert ist. Über elektrochemische Eigenschaften hinaus müssen die Elektroden eine gute Haftfestigkeit auf dem Substrat aufweisen, damit sich die MEAs nach einem Experiment mit einer Zellkultur reinigen und sterilisieren und somit wiederverwenden lassen.
Fertigung und Experimente
Als Ausgangssystem und MEA-Referenz diente ein Standard-MEA mit 59 Arbeitselektroden aus kolumnaren Titannitrid (TiN) mit einem Durchmesser von je 30 µm in einem Abstand von 200 µm in quadratischer 8 x 8-Anordnung, sowie eine Referenzelektrode auf. Die Elektroden sind über Titanleiterbahnen mit am Rande des Float-Glassubstrates (Größe 5 cm x 5 cm) angeordneten Kontaktpads verbunden. Als Isolator kommt eine Siliziumnitrid (SiN)-Schicht zum Einsatz. Die Strukturierung des Leiterbahn-Elektroden-Systems und der Isolatorschicht erfolgt photolithographisch mit nasschemischen Ätzverfahren der Leiterbahnen und trockenchemischen Ätzverfahren des Isolators.
Für die Versuche zur Synthese von CNTs wurden TiN-Elektroden auf einem temperaturstabilen Quarzglas abgeschieden. Der ursprüngliche Leiterbahn-Isolator-Aufbau erwies sich dabei jedoch als nicht geeignet, da aufgrund der bei der Synthese auftretenden Temperaturen in Höhe von 600 °C bis 650 °C die Isolationsschicht aufbrach. Die Ursache hierfür ist eine Kombination aus recht unterschiedlichen thermischen Ausdehnungskoeffizienten der verwendeten Materialien (αTi = 10,37·10-6/K [2],
αSiN = 1,6·10-6/K [3]) und aus der Tatsache, dass bei hohen Temperaturen Wasserstoff aus der Siliziumnitridschicht herausdiffundiert, welcher das Auftreten von Rissen begünstigt [4].
Zur Lösung dieses Problems wurde ein temperaturstabiles Leiterbahn-Isolatorschichtsystem mit TiN-Leiterbahnen und SiOx-Isolatorschicht entwickelt (Abb. 2). Diese beiden Materialien haben mit αTiN = 9,0·10-6/K [5] und αSiO = 8,5·10-6/K [6] deutlich näher beieinander liegende thermische Ausdehnungskoeffizienten. Dieses Schichtsystem blieb auch nach dem Hochheizen auf bis zu 900 °C mechanisch stabil und behält auch nach dieser thermischen Belastung seine Isolationseigenschaften. Das Titannitrid hat zudem die zur CNT-Synthese notwendige Eigenschaft einer Diffusionsbarriere für die Katalysatorschicht.


Abb. 2: Prozessschema der MEA-Herstellung. 1.) Aufsputtern von TiN, 2.) Belacken, Belichten und Entwickeln der 1. Photolackschicht, 3.) Strukturierung der Leiterbahnen via Trockenätzen, 4.) Abscheiden einer SiO-Schicht, 5.) Belacken, Belichten und Entwickeln der 2. Photolackschicht, 6.) Strukturierung des Isolators, 7.) Abdecken der freigeätzten Kontaktpads mit Photolack, 8.) Aufsputtern des Katalysators, 9.) Lift-Off des Katalysators, 10.) Synthese der CNT-Elektroden und 11.) Anwenden eines O2-Plasmas
Das Titannitrid wurde in einer PVD-Anlage reaktiv auf die Quarzglassubstrate aufgesputtert. Zur Strukturierung des Titannitrids in Leiterbahn-, Elektroden- und Kontaktpad-Struktur wurde nach erfolgter Strukturierung der Lackmaske ein neu entwickelter Trockenätzprozess angewandt. Zum Entfernen des Lackes wurden die Substrate für mindestens 12 Stunden in 80 °C heißes Lösungsmittel eingelegt.
Die SiOx-Isolatorschicht stammt aus einem plasmaverstärkten CVD (PECVD-) Prozess mit Distickstoffmonoxid (N2O) und Monosilan (SiH4) als Ausgangsstoffen. Die Strukturierung der Isolatorschicht, das heißt die Öffnung der Isolatorschicht über Elektroden und Kontaktpads, erfolgte ebenfalls mittels eines Trockenätzprozesses. Der zur CNT-Synthese notwendige Katalysator wurde nach dem Abdecken der Kontaktpads auf das MEA-Substrat aufgesputtert. Es wurden hierfür 10 nm Nickel verwendet, welche über einen finalen Lift-Off-Prozess in einer Acetonlösung derart strukturiert wurden, dass nur die Elektrodenfläche mit Nickel versehen ist. Die Strukturierung der Katalysatorschicht entspricht der Strukturierung der CNT-Schicht.
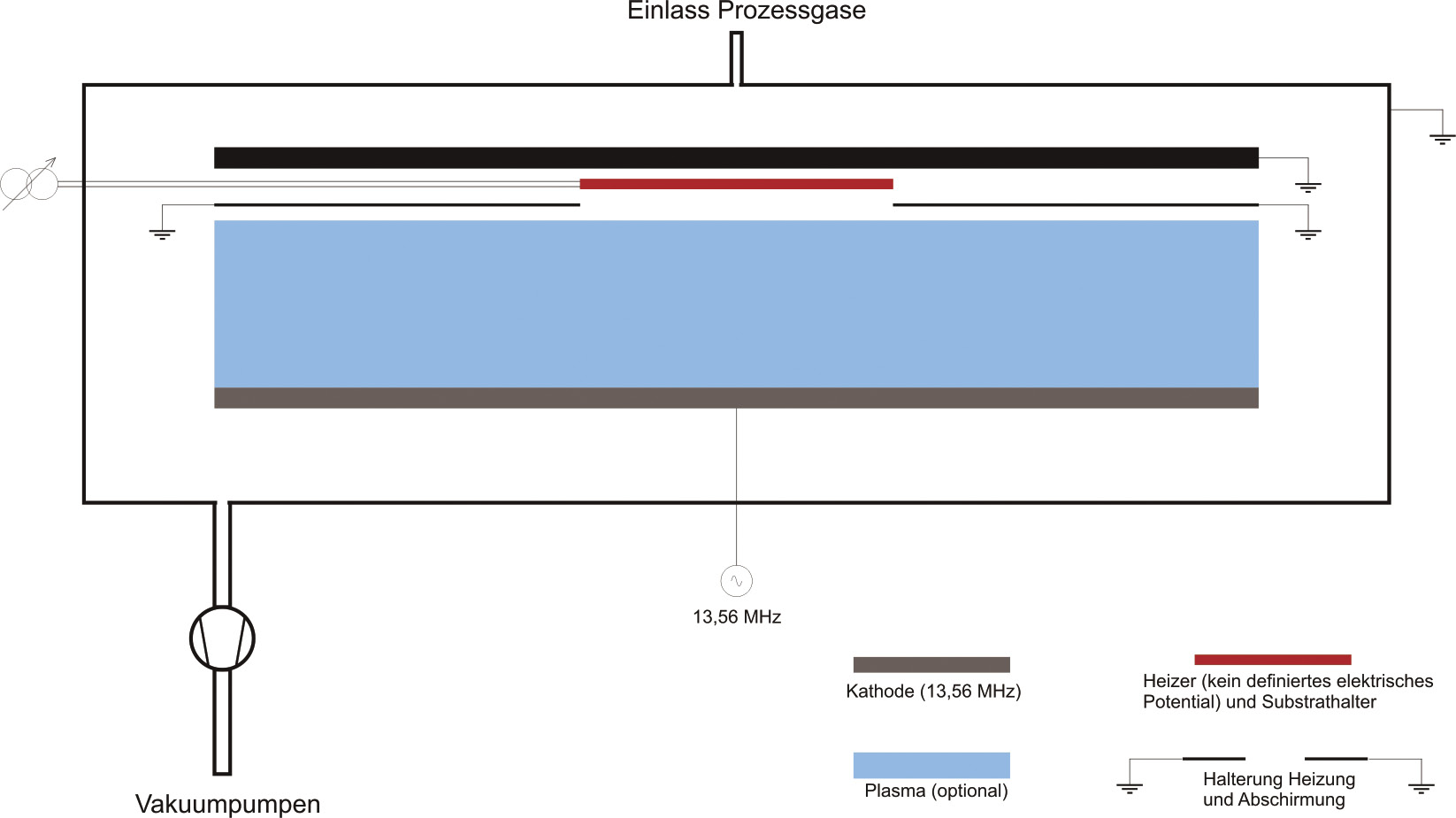
Abb. 3: Anlagenschema des um einen Keramikheizer erweiterten Vakuumrezipienten
Die CNT-Synthese erfolgte in einem modifizierten Vakuumrezipienten, welcher hierfür mit einem von einem Trenntransformator gespeisten Keramikheizelement nachgerüstet wurde (Abb. 3 – Anlagenschema). Die Temperaturmessung erfolgt über ein Thermoelement vom Typ K (NiCr-Ni). Die CNT-Synthese erfolgt nach Hochheizen des MEA-Substrates auf eine Temperatur von 630 °C in einer Ammoniak-Acetylen- (NH3-C2H2) Gasatmosphäre. Eine 5-minütige Prozessdauer resultiert bei diesen Parametern in einer CNT-Höhe von etwa 15 µm (Abb. 4 und Abb. 5).

Abb. 4: CNT-Mikroelektrodenarray in 150-facher Vergrößerung nach Synthese der CNT-Elektroden

Abb. 5: Nahaufnahme einer CNT-Elektrode [8]
In einem letzten Prozessschritt wird mittig auf das MEA-Substrat ein Glasring aufgeklebt, welcher in späteren Versuchen als Zellkulturgefäß dient.
Charakterisierung
Zur Charakterisierung der CNT-Elektroden wurden deren Impedanz bei der Frequenz von 1 kHz und deren Ladungsübertrag bei Spannungspulsen bis 1 V gemessen. Hierzu wird der Verlauf des Stromes während eines 500 µs langen Spannungspulses gemessen. Das Zeitintegral dieses Stromverlaufes entspricht der übertragenen Ladung. Ihr Maximalwert Qmax am Ende des Pulses wird zur Charakterisierung von Stimulationselektroden herangezogen.
Vor diesen elektrochemischen Messungen wurden die CNT-Elektroden für 1 Sekunde einem O2-Plasma ausgesetzt. Grund hierfür ist eine dünne Schicht amorphen Kohlenstoffs, welche unmittelbar nach der Synthese die CNTs umgibt und zu hohen Impedanzwerten führt [7]. Das O2-Plasma ätzt diese Kohlenstoffschicht weg und erniedrigt die Impedanzen um eine Größenordnung.
Für MEAs mit CNT-Elektroden (CNT-MEA) wurde eine Impedanz in Höhe von 20 kΩ gemessen. Im Vergleich hierzu liegt die Impedanz von Standard-MEAs mit TiN-Elektroden unter gleichen Messbedingungen bei 40 kΩ. Eine ähnlich deutliche Verbesserung zeigt sich bei den vergleichenden Messwerten des maximalen Ladungsübertrages: Hier erreichen CNT-Elektroden einen Ladungsübertrag von 10,1 nC anstatt 5,9 nC bei TiN-Elektroden (Abb. 6).

Abb. 6: Maximaler Ladungsübertrag Qmax von CNT- und TiN-Elektroden (jeweils 30 µm Durchmesser) in Abhängigkeit von der Amplitude mit Spannungspulsen von 500 µs Dauer. Bei der Spannung von +1 V ist der maximale Ladungsübertrag einer CNT-Elektrode mit 10,1 nC im Vergleich zur herkömmlichen TiN-Elektrode mit 5,9 nC um 71 % erhöht [8]
Zur Überprüfung der Biokompatibilität und der Tauglichkeit der CNT-MEAs zum Aufzeichnen extrazellulärer elektrischer Signale wurden Zellkulturtests durchgeführt. Hierfür wurden Kulturen von Neuronen aus dissoziierten Hirnpräparaten von Ratten auf den MEAs verwendet. Zuvor wurde der CNT-MEA zur Sterilisation für 12 Stunden UV-Licht ausgesetzt. Die Zellen wurden in das Zellkulturgefäß auf dem CNT-MEA einpipettiert, bei 37 °C in einem Brutschrank gelagert und drei mal pro Woche zum Wechsel des Nährmediums sowie für Messungen zellulärer Aktivität aus dem Brutschrank herausgenommen (Abb. 7).

Abb. 7: Schematische Darstellung eines MEA mit Zellkulturgefäß, Zellkultur und Elektrolytlösung (PBS, Phosphate Buffered Saline)
Die Zellkultur auf dem CNT-MEA konnte für den verhältnismäßig langen Zeitraum von 12 Wochen aufrecht erhalten werden. Die Neuronen zeigten während dieser Zeit messbare elektrische Zellaktivität, so genannte Spikeaktivität (Abb. 8). Die kultivierten Nervenzellen bilden auf den CNT-MEAs Netzwerke aus, was sich an der synchronen Aktivität in der Multi-Elektroden-Ableitung in Abbildung 9 und Abbildung 10 zeigt. Die Biokompatibilität sowohl der neu verwendeten SiOx-Isolatoroberfläche als auch der CNT-Elektroden und deren generelle Tauglichkeit für die Verwendung in neuronalen Zellkulturen kann somit als gegeben betrachtet werden.

Abb. 8: Elektrische Aktivität von kultivierten Nervenzellen (Kortexneurone, Ratte), gemessen mit einem CNT-MEA. Die Spannungsspitzen (Spikes) in Höhe von -40 µV bis +40 µV lassen sich klar vom 10 µV starken Rauschlevel unterscheiden. Mit diesen Werten ergibt sich ein Signal-zu-Rausch-Verhältnis von 8:1 (peak-to-peak) [8]

Abb. 9: Multi-Elektroden-Ableitung mit einem CNT-MEA. In der unteren Bildhälfte markieren die Punkte die Spikes, die mit den 59 Elektroden des MEAs während eines Zeitfensters von 300 s gemessen wurden. Die Nummerierung der vertikalen Achse (1 bis 60) entspricht der Anzahl der Elektroden (59 Arbeitselektroden + Referenzelektrode). In der oberen Bildhälfte wurden die Spikes aller Elektroden in einem Histogramm zusammengefasst, um synchrone Aktivität im Netzwerk zu ermitteln. Die Messung wurde zwei Wochen nach dem Anlegen der Zellkultur vorgenommen. Die Vernetzung der Neurone ist hier noch unvollständig: Nicht auf allen Elektroden ist gleichzeitig ein Spike messbar

Abb. 10: Histogramm der gemessenen Spikeaktivität sieben Wochen nach dem Anlegen der Zellkultur auf einem CNT-MEA, gemessen in einem Zeitfenster von 300 s. Hier ist im Vergleich zu Abbildung 9 eine ausgeprägte Vernetzung der Neurone zu erkennen: Nahezu alle Elektroden registrieren gleichzeitig Spike-Aktivität oder gleichzeitig keine Spike-Aktivität
In einer weiteren Versuchsreihe wurde ein CNT-MEA autoklaviert und im Anschluss seine Impedanz gemessen. Diese war im Vergleich zur anfänglichen Impedanz vor dem Autoklavieren um etwa 20 % erhöht, blieb jedoch deutlich unter der für die MEA-Tauglichkeit akzeptierten Grenze von 100 kΩ. In zwei weiteren Autoklaviervorgängen blieb die Impedanz auf diesem Niveau stabil und erhöhte sich nicht weiter.
Zusammenfassung
Für neuronale MEA-Anwendungen wurden CNTs zur Nutzung als Mikroelektrode synthetisiert. Aufgrund der hohen Temperaturen (630 °C) bei der Synthese kam statt des konventionellen, nicht-temperaturstabilen Ti-SiN Leiterbahn-Isolator-Schichtsystems der MEAs ein neu entwickeltes, temperaturstabiles TiN-SiOx Leiterbahn-Isolator-Schichtsystem samt dazugehöriger neu entwickelter Lithographieprozesse zum Einsatz. Elektrochemische Messungen der CNT-Elektroden ergaben eine um 50 % verringerte Impedanz bei gleichzeitig 71 % höherem maximalen Ladungsübertrag im Vergleich zu TiN-Elektroden. Der CNT-MEA erwies sich in 12-wöchigen Zellkulturtests mit Nervenzellen biokompatibel. Netzwerkbildung der Neuronen und deren gut messbare elektrische Zellaktivität belegen die Tauglichkeit von CNT-Elektroden für neuronale MEA-Anwendungen. Die CNT-MEA lassen sich autoklavieren und sind somit wiederverwendbar.
Literatur
[1] A. Stett, U. Egert, E. Guenther, F. Hofmann, T. Meyer, W. Nisch, H. Haemmerle: Biological application of microelectrode arrays in drug discovery and basic research, Analytical and bioanalytical chemistry, 377(3):486-495, 2003
[2] K. Akagi, Y. Okamoto, T. Matsuura, T. Horibe: Properties of test metal ceramic titanium alloys, the Journal of prosthetic dentistry, 68(3):462-467, 1992
[3] T. F. Retajczyk, A. K. Sinha, et al.: Elastic stiffness and thermal expansion coefficients of various refractory silicides and silicon nitride fims, Thin Solid Films, 70(2):241-247, 1980
[4] M. Gupta, V. K. Rathi, R. Thangaraj, O. P. Agnihotri, K. S. Chari: The preparation, properties and applications of silicon nitride thin fims deposited by plasma-enhanced chemical vapor deposition, Thin Solid Films, 204(1):77-106, 1991
[5] J. Mukerji, S. K. Biswas: Synthesis, properties, and oxidation of alumina-titanium nitride composites, Journal of the American Ceramic Society, 73(1):142-145, 1990
[6] F. Jansen, M. A. Machonkin, N. Palmieri, D. Kuhman: Thermal expansion and elastic properties of plasma-deposited amorphous silicon and silicon oxide fims, Applied physics letters, 50(16):1059-1061, 1987
[7] H. C. Su, C. M. Lin, S. J. Yen, Y. C. Chen,
C. H. Chen, S. R. Yeh, W. Fang, H. Chen, D. J. Yao, Y. C. Chang, et al.: A cone-shaped 3d carbon nanotube probe for neural recording, Biosensors and Bioelectronics, 26(1):220-227, 2010
[8] B. Stamm, K. Schneider, T. Herrmann, M. Fleischer, C. Burkhardt, W. Nisch, D. P. Kern, A. Stett: Carbon nanotube electrodes for neuronal recording and stimulation, Proceedings MEA Meeting 2012, 280-281, 2012
Kontakt:
boris.stamm@nmi.de
- www.nmi.de
DOI:10.7395/2012/Stamm1





