Kategorien
Metallabscheidung – galvanisch26.07.2018
Als galvanische Metallabscheidung wird die Umwandlung von gelöstem Metall in den festen Metallzustand durch Einsatz von elektrischem Strom über einen äußeren Stromkreis bezeichnet. Die galvanische Metallabscheidung erfolgt in den meisten Fällen aus einer wässrigen Lösung eines Metallsalzes – z. B. Nickelchlorid, Nickelsulfat, Kupfersulfat, Zinkchlorid. Die wässrige Lösung enthält neben dem gelösten Metallsalz je nach Art der Metallabscheidung zusätzlich Stoffe zur Erzeugung eines stabilen Säuregrades (pH-Wert), zur Herstellung von glatten und glänzenden Metallschichten (Glanzbildner) oder auch zur Verbesserung der elektrischen Leitfähigkeit (Leitsalze) der wässrigen Lösung. Die Abscheidung von Metall erfolgt, indem die positiv geladenen Metallionen – z. B. zweifach positiv geladenen Nickelionen (Ni2+) oder zweifach positiv geladene Kupferionen (Cu2+) – an der als Kathode bezeichneten Elektrode zum reinen Metall reduziert werden. Zur Erzeugung des notwendigen Stromkreises befindet sich im selben Behältnis eine zweite Elektrode (Anode), an der der umgekehrte Prozess abläuft und ein Metall durch den Entzug von Elektronen aus dem Metall ein Metallion entsteht: Nickel wird zum Nickelion (Ni2+). Für diesen Prozess wird in den meisten Fällen Gleichstrom verwendet. Die Höhe des Stroms hängt von der Größe der Oberfläche ab, die mit einer galvanisch abgeschiedenen Metallschicht überzogen wird. Je nach Art und Eigenschaft des abgeschiedenen Metalls liegen die Stromdichten (Strom pro Abscheidefläche) bei Werten zwischen 0,1 A/dm2 und bis zu 100 A/dm2; in Ausnahmefällen auch darunter oder darüber. Daraus ergeben sich Abscheidegeschwindigkeiten zwischen 0,1 µm pro Minute und bis zu 10 µm pro Minute. Unterschiede ergeben sich vor allem aufgrund unterschiedlicher Ladungszahlen der eingesetzten Metallionen (Wertigkeit der Elemente – zwischen einer und bis zu sechs Elementarladungen) sowie dem Anteil an unerwünschten Nebenreaktionen, im Falle der Metallabscheidung ist dies zum Beispiel die Wasserstoffentwicklung.
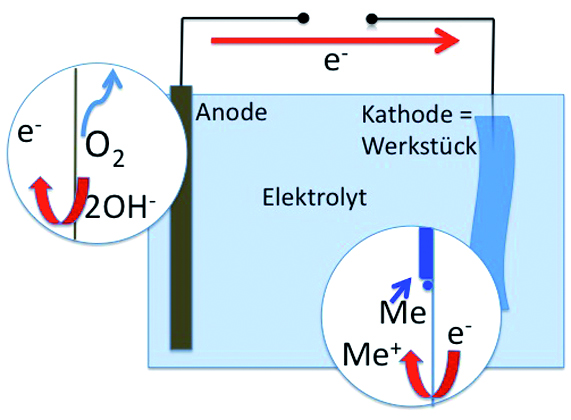
Prinzip der galvanischen Abscheidung
Die galvanische Metallabscheidung zeichnet sich unter anderem dadurch aus, dass die unterschiedlichsten Metallkombinationen aus Grundmaterial und Beschichtung aufgebaut werden können und dadurch dem Grundmaterial unterschiedliche zusätzliche Eigenschaften verliehen werden können. Die Metallschichten lassen sich des Weiteren relativ gleichmäßig auf alle Bereiche auftragen, die mit der wässrigen Lösungen (Abscheideelektrolyten) in Kontakt sind und nicht vollständig vom elektrischen Feld des Abscheidestrom abgeschirmt sind. An Punkten mit höhere Feldstärke (Ecken, Kanten, Spitzen) wird bei vielen Elektrolyttypen mehr Metall abgeschieden, als in Vertiefen. Daraus ergeben sich dann Unterschiede in der Schichtdicke, die bei Teilen mit geringen Passungstoleranzen zu berücksichtigen sind. Ein wesentlicher Vorteil der galvanischen Abscheidung ist der außerordentlich effiziente und sparsame Einsatz von Metallen. Mit geringsten Mengen an Metall wird einem Grundwerkstoff eine bestimmt Eigenschaft verliehen. So werden beispielsweise Eisenwerkstoffe gegen Korrosion durch galvanische Zinkschichten mit Dicken zwischen 10 µm und 15 µm geschützt. Ein Bauteil mit einer Oberfläche von 1 m2 verbraucht bei einer Dicke der Zinkschicht von 15 µm lediglich 107 g Zink. Das im Prozess gelöste Zink kann vollständig aufgearbeitet werden, so dass daraus praktisch kein Verlust entsteht. Mit Hilfe von speziellen Abdecktechniken lassen sich zudem bei nahezu allen galvanischen Verfahren die Schichten auch partiell dort aufbringen, wo sie ihre Funktion erfüllen müssen (Anmerkung: 1000 µm = 1 mm).