Bald Brennstoffe aus Kohlendioxid?
Kohlenwasserstoffe sind immer noch unsere bedeutendsten Energieträger, aber müssen sie zwangsläufig aus fossilen Quellen gewonnen werden? Warum nicht den Verbrennungsprozess umkehren und sie aus Kohlenstoffdioxid aufbauen? Dies ließe sich mit einem durch Sonnenenergie getrieben Verfahren realisieren, sobald geeignete Katalysatoren zur Verfügung stehen. Wissenschaftler aus Japan und China stellen in der Zeitschrift Angewandte Chemie jetzt ein neues, besonders effektives photokatalytisches System vor – vielleicht ein weiterer Schritt auf dem Weg zu Kohlenstoffdioxid-neutralen Kraft- und Brennstoffen.

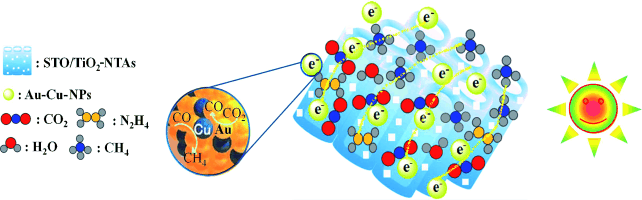
Bestrahlung mit Sonnenlicht setzt Elektronen in den Halbleiterröhrchen frei. Diese werden auf die bimetallischen Edelmetallnanopartikel übertragen und von dort weiter auf das Kohlenstoffdioxid / Bildquelle: Wiley-VCH
Verschiedene Katalysatoren für die photokatalytische Reduktion von Kohlenstoffdioxid wurden bereits entwickelt, beispielsweise auf der Basis von Strontiumtitanat (SrTiO3, STO) oder Titandioxid (TiO2). Angesichts der speziellen Energieniveaus dieser zwei Halbleitermaterialien schien den Forschern um Jinhua Ye eine Heterostruktur aus beiden Stoffen besonders erfolgversprechend. Die Wissenschaftler vom National Institute for Materials Science (Japan) und dem U-NIMS Joint Research Center der Tianjin University (China) stellten Anordnungen koaxial ausgerichteter STO/TiO2-Nanoröhrchen her. Die Röhrchen bestückten sie gleichmäßig mit Nanopartikeln aus einer Gold-Kupfer-Legierung als Cobalt-Katalysator. Hydrazin-Hydrat (N2H4 • H2O) dient als Wasserstoffquelle und sorgt für die notwendige reduzierende Atmosphäre. So gelang es den Forschern, Kohlenstoffdioxid sehr effizient in Kohlenstoffmonoxid, Methan (CH4) und weitere Kohlenwasserstoffe umzusetzen.
Bestrahlung mit Sonnenlicht setzt Elektronen in den Halbleiter-Röhrchen frei. Dank der STO/TiO2-Heterostrukturen lässt sich die damit verbundene Ladungstrennung besser aufrecht erhalten als bei den reinen Substanzen. Die Elektronen werden auf die bimetallischen Edelmetallnanopartikel übertragen und von dort weiter auf das Kohlenstoffdioxid, das entstehende Kohlenstoffmonoxid und weitere gasförmige Zwischenprodukte. Die hohe Oberfläche der Röhrenbündel und die Porosität der Wände der Nanoröhrchen sorgen für eine hohe Gasdiffusion und sorgen für einen effektiven Transport der Ladungen. Aufgrund spezieller Legierungseffekte können die Gold-Kupfer-Nanopartikel den Rücktransport photogenerierter Elektronen in den Halbleiter wesentlich effektiver aufhalten als die Reinmetalle. Das Hydrazin-Hydrat liefert den benötigten Wasserstoff, sorgt für einen Elektronennachschub am Katalysator und schafft eine reduzierende Atmosphäre, die die Metallnanopartikel über lange Zeit stabilisiert. Wird dagegen Wasser als Wasserstoffquelle genutzt, ist eine rasche Deaktivierung des katalytischen Systems zu verzeichnen. Das Kohlenstoffdioxid wird an den Nanopartikeln zunächst zu Kohlenstoffmonoxid und dann weiter zu CH4 und anderen Kohlenwasserstoffen reduziert. Bei einem Verhältnis von Gold zu Kupfer von 3:1 in der Legierung ist der Anteil der entstehenden Kohlenwasserstoffe am höchsten.
Aktuelle Onlineartikel
-

11. 05. 2026 Fluorfreie Trockenbeschichtung für leistungsfähige Batterien
-

11. 05. 2026 Laserdirektplattieren senkt Taktzeit und Kosten für dicke Metallbeschichtungen
-
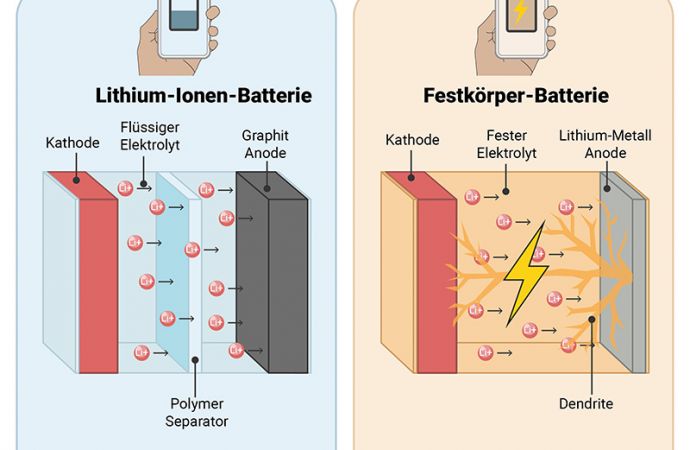
27. 04. 2026 Warum kommt es zu Kurzschlüssen in Festkörper-Batterien?
-

27. 04. 2026 Neuer internationaler Masterstudiengang „Battery Technologies“ startet zum Wintersemester 2026/27
-

27. 04. 2026 Nanofiltration – Wasser wirksam von Glyphosat befreien
-

22. 04. 2026 ZVO-Oberflächentage 2026 erstmals in Karlsruhe: Jetzt anmelden!