Fachwissen aus Werkstoffkunde und Oberflächentechnik
– für alle, die ihr Wissen auffrischen oder neues erwerben wollen
– für Fachfremde, Auszubildende oder Praktiker
•Als Abonnent haben Sie auf www.womag-online.de Zugriff auf die gesamten Fachtexte in voller Länge. Der Stoff wird laufend erweitert und ist online ohne Einschränkung verfügbar!
Werkstoffe als Basis für Bauteile – Chemische Bindungsarten
Atombindung
Unpolare Atombindung
Atombindungen, auch kovalente Bindungen oder Elektronenpaarbindungen genannt, entstehen bei der Reaktion von zwei Nichtmetallatomen. Da diese schon mehr als 4 Elektronen auf der Außenschale haben (außer Wasserstoff), sind sie nicht bereit in einen lonenzustand überzugehen, das heißt Elektronen abzugeben. Es erfolgt kein vollständiger Elektronenübertrag. Sie gehen eine Verbindung ein, in dem sie so nahe zusammenrücken, dass ein Überlappungsbereich der Valenzschalen entsteht, das heißt jedes der Atomkerne betrachtet die gemeinsame, äußere Schale als seine eigene.
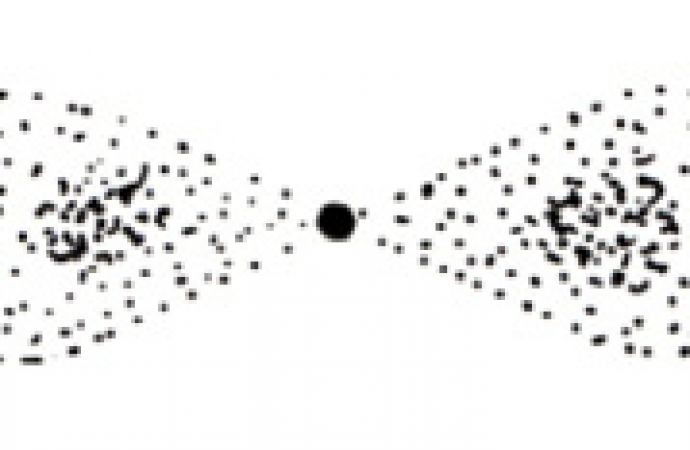
Die Grundlage für das Verständnis der Atombindung ist die Elektronenverteilung in der Außenschale. Sie lassen sich mit Hilfe des so genannten Orbitalmodels recht anschaulich erklären. Eine Möglichkeit der Form ist die Elektronenwolke, die ihre größte Dichte auf einer Kugeloberfläche hat, die so genannte s-WoIke (s-Orbital). Eine andere Form ist die so genannte p-WoIke (p-Orbital), die die Form einer um die Langsachse rotierenden Acht aufweist (Abb. 36 und 37).

Abb. 36: Aufenthaltswahrscheinlichkeit der Elektronen in der s-Wolke

Abb. 37: Aufenthaltswahrscheinlichkeit der Elektronen in der p-Wolke
Bei der Atombindung binden sich die Atome. Man stellt sich das so vor, dass die Elektronenpaare, die sich bei der Atombindung bilden, in einer Achterschleife beide Atomkerne umkreisen. Auf diese Weise gehört jedes Valenzelektron zu zwei Atomkernen. Der einfachste Fall einer Atombindung ist das Wasserstoffmolekül. Wenn die zwei Atome zusammenkommen, überlappen sich ihre Atomorbitale derart, dass die Elektronenwolke im Bereich zwischen den Atomkernen dichter wird. Die erhöhte negative Ladungsdichte in diesem Bereich zieht die positiv geladenen Atomkerne an. Auch hier gilt das Pauli Prinzip: Die beiden Elektronen haben einen entgegengesetzten Spin. Die zwei Wasserstoffatome haben ihre Elektronen so überlagert, dass sich eine annähernd schalenförmige Wolke bilden kann. Nur sind jetzt in der Wolke zwei Atomkerne vorhanden. Da nur ein Elektron von jedem Atom an der Bindung beteiligt ist, entsteht eine Einfachbindung (ein Elektronenpaar) (Abb. 38 und 39).

Abb. 38: Aufenthaltswahrscheinlichkeit der Elektronen im Wasserstoffmolekül

Abb. 39: Modelldarstellung der Wasserstoffmolekülbildung
Chemische Schreibweisen
Symbolisch wird für das Wasserstoffmolekül eine Darstellung mit Punkten oder Strichen verwendet (H : H oder H–H in Abb. 40). Dabei symbolisieren die beiden Punkte die Elektronen, die an der Bindung beteiligt sind, wobei die 2 Punkte das gemeinsame Elektronenpaar darstellen. Gebräuchlicher ist die Schreibweise, in der ein Bindungsstrich für das gemeinsame Elektronenpaar verwendet wird. Die Elektronen werden jetzt dem Gesamtmolekül zugeordnet, das heißt jedes Wasserstoffatom ist an zwei Elektronen beteiligt und hat damit eine Elektronenkonfiguration, die derjenigen des Edelgases Helium entspricht.

Abb. 40: Schreibweise der Wasserstoffbildung
Chemische Formeln, so auch die Moleküle, können in 3 Darstellungsvarianten geschrieben werden: als Summenformel, Strukturformel oder rationelle Formel (Halbstrukturformel).
In der Summenformel werden alle Elemente und die Anzahl der beteiligten Atome beschrieben (Summenformel des Wasserstoffmoleküls: H2). Die Strukturformel gibt auch die Elemente und deren Anzahl an, sie zeigt aber zusätzlich, wie die Elemente miteinander verknüpft sind (Strukturformel des Wasserstoffmoleküls: H–H). Bei größeren Molekülen ist daraus die Anordnung der einzelnen Atome im Raum (Raumstruktur) ersichtlich.