Teil 2: CO2-Reduktion an Metalloxidoberflächen, Beispiele, Anlagentechnik
Metalloxide und ihre Kombination mit katalytisch wirkenden Metallpartikeln bieten ein vielfältiges System photokatalytisch wirksamer Werkstoffe. Solche Systeme werden heute vielfach im Labor erforscht, die für eine praktische Umsetzung wichtigen Systemfragen finden dabei wenig Beachtung. Einige Anwendungsbeispiele zeigen die Bandbreite möglicher Werkstoffkombinationen auf.
Photoelectrochemical Reduction of Carbon Dioxide at Interfaces
Part 2: CO2 Reduction at Metal Oxide Surfaces, Examples and Plant Technology
Metal oxides and their combination with catalytic metal particles offer a variable system of photocatalytic materials. Such systems are investigated in the lab by many groups today. The development of system aspects which are important for the practical implementation is seldom addressed. Some practical examples will show the breadth of possible material combinations for practical solutions.
Im ersten Teil des vorliegenden Artikels wurde zunächst ein Überblick über Reaktionswege der Kohlendioxidreduktion gegeben und verschiedene Klassen von Katalysatorsystemen wurden vorgestellt. Es schlossen sich grundlegende Betrachtungen zu den Reaktionsmechanismen in wässrigen und nicht wässrigen Reaktionsmedien an. Je nachdem, ob es sich um organische oder anorganische Lichtsammler und Katalysatoren handelt, erfolgt die Umwandlung von Kohlenstoffdioxid (CO2) in Kohlenwasserstoffe über ganz unterschiedliche Wege. Es können Methan, Formiat oder Methanol oder auch Mischungen dieser Produkte entstehen, je nach Selektivität des Katalysators und den äußeren Reaktionsbedingungen.
Im zweiten Teil des Artikels sollen nun einige Besonderheiten von Metalloxiden als Lichtsammler und Träger von Katalysatorpartikeln dargestellt werden.
3 Besonderheiten an halbleitenden Metalloxidoberflächen
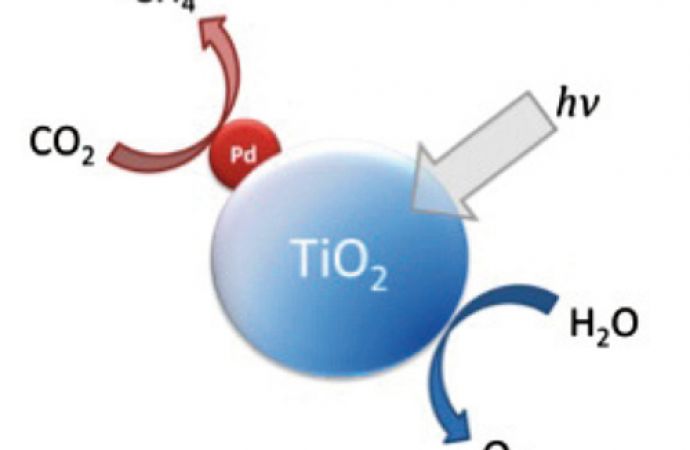
Bei der Reduktion von Kohlendioxid ist die Erzeugung eines CO2-Radikals (CO˙2-) der Schritt mit dem höchsten Energiebedarf. Das Radikal ist sehr reaktionsfreudig und reagiert in wässrigen Medien meist zu Methanol, in nicht wässrigen Medien entstehen bevorzugt Formiat und Kohlenstoffmonoxid. Um die hohen Energien zur Radikalbildung bereitzustellen, hat sich eine Kombination von Halbleitern mit möglichst kleinen, an der Oberfläche befindlichen Metallpartikeln als gut geeignet erwiesen (Abb. 3). Die Halbleiter sammeln die Photonen und erzeugen energiereiche Elektronen. Die an den Metallpartikeln gesammelten Elektronen können dort katalytisch wirken [3].
Oft werden die Halbleiter auch mit Metallen dotiert, beispielsweise erzeugen Titandioxidpartikel mit 3 % Kupferoxid selektiv Methanol aus Kohlenstoffdioxid. Auch Platin-nano-Inseln mit einem Durchmesser von 5 nm bis 30 nm auf Titandioxid (TiO2) erlauben die Erhöhung der Reaktionsraten bei der Herstellung von Wasserstoff aus Wasser um mehrere Größenordnungen. Aus der Art des Halbleitermaterials, der genutzten oder nutzbaren Lichtwellenlänge sowie dem eingesetzten Katalysator entsteht so ein System mit extrem vielen Variationsmöglichkeiten. Allerdings sind auch viele Metalloxide selbst katalytisch aktiv, neben dem bekannten Titandioxid sind hier beispielsweise Lanthan-Titan-Oxid (La2Ti2O7) oder Strontium-Niob-Oxid (Sr2Nb2O7) zu nennen.
Oberflächenkatalysatoren auf Metalloxidpartikeln erlauben sehr effiziente Reaktionen zur Herstellung von solaren Energieträgern. Für den Transport der energiereichen Elektronen zu den metallischen Katalysatorzentren ist eine hohe Kristallinität und spezifische Oberfläche der Partikel erforderlich. Die Präparation solcher Metalloxidpartikel kann entweder über Festkörper oder aber über Salzschmelzen, wie beispielsweise Mischungen aus Natrium- und Kaliumchlorid (NaCl/KCl) oder Natrium- und Kaliumsulfat (Na2SO4/K2SO4) erfolgen. Bei der Synthese in Salzschmelzen lassen sich Partikelgröße und Partikelmorphologie sowie die Art der nach außen gerichteten Kristallflächen gezielt einstellen. Partikel aus La2Ti2O7 oder aus lanthandotiertem Natrium-Tantal-Oxid (NaTaO3), die in einer Salzschmelze hergestellt wurden, zeigen eine bis zu zweifach höhere photokatalytische Reaktionsrate als Partikel aus Festkörperprozessen [2].
Viele Oxidpartikel der ersten Übergangsmetalle zeigen eine hohe Effizienz beim Einfangen von UV-Strahlung und bei der Separierung der erzeugten Elektron-Loch-Paare. Allerdings entsprechen die jeweils erreichbaren photokatalytischen Reaktionsraten nicht der Umwandlungseffizienz bei den Lichtquanten aus dem sichtbaren Spektrum. Die genauen Ursachen hierfür und die Details der Reaktionsmechanismen sind Gegenstand aktueller Forschung.
Die Ergebnisse der bisherigen Forschungsarbeiten zeigen, dass zukünftig eine Präparationstechnik benötigt wird, die ein Feintuning von Oberflächenmorphologien und Reaktionszentren erlaubt. Neue Werkstoffe sind beispielsweise Kupfer(I)-Niobat oder Kupfer(I)-Tantalat, deren Bandenergien gut zu den Redoxreaktionen passen, die zur Herstellung von solaren Energieträgern wichtig sind.
4 Beispiele verschiedener Reaktionssysteme
Es gibt heute Tausende von Forschungsartikeln über die photokatalytische Reduktion von Kohlenstoffdioxid an den verschiedensten Materialien. Eine Suche nach diesen Begriffen auf Google Scholar liefert 10 500 Ergebnisse. Aus dieser Vielfalt sollen drei Beispiele die Möglichkeiten und die Bandbreite der chemischen Systeme bei anorganischen Photomaterialien ein wenig illustrieren – ohne jeden Anspruch auf Vollständigkeit.
Die Methanolherstellung aus Kohlenstoffdioxid mit Hilfe von CuInS2 beschreiben Yuan und Hao [4]. Dieses Material wurde auch schon für photovoltaische Zellen beschrieben, seine Bandlücke passt sehr gut zum solaren Spektrum und erlaubt die Nutzung des sichtbaren Anteils der Sonnenstrahlung. Zur Präparation wurde zunächst Cu2In aus einem Elektrolyt mit 5 mmol/l CuCl2, 5 mmol/l InCl3, 0,2 mmol/l Triethanolamin und 0,015 mmol/l Natriumcitrat bei pH = 4 galvanisch abgeschieden. Die Schicht wurde dann in einem Rohrofen zusammen mit Schwefel unter Stickstoff bei 400 °C für eine halbe Stunde sulfuriert. Diese Photokathode kann Kohlenstoffdioxid reduzieren. Für die Versuche zur Umwandlung von Kohlenstoffdioxid wurde der Halbleiter in ein Arbeitsmedium aus Wasser mit 10 mmol/l Pyridin (Abb. 4) und einem Citratpuffer gegeben und bestrahlt.
![]()
Abb. 4: Chemische Struktur von Pyridin
Dabei wird das Pyridin an der Photokathode reduziert (Abb. 5) und die entstehenden Ionen können Kohlenstoffdioxid zum CO˙2--Ion reduzieren. Das Pyridin reduziert die Überspannung dieser ersten Reduktionsreaktion und wirkt als Katalysator. Dies wurde durch Konzentrationsmessungen zu Beginn des Versuches und nach einiger Zeit bestätigt. Nach der Vorstellung der Autoren bildet das Pyridinion mit dem Kohlenstoffdioxid zusammen ein Carbamat, welches dann weiter bis zum Methanol reagiert. Durch den Katalysator entsteht kein Wasserstoff an der Photokathode, obwohl dieser nur eine sehr geringe Überspannung hat. Die Stabilität der Kathode über einen Zeitraum von elf Stunden war sehr gut. Weitere Daten liegen nicht vor.
Einen ganz anderen Halbleiter, aber ein ähnliches chemisches System haben Barton et. al. eingesetzt [5]. Galliumphosphid hat eine sehr gute Selektivität für die Erzeugung von Methanol aus Kohlenstoffdioxid, allerdings bei einer hohen Überspannung. Das Redoxpotential für die Kohlenstoffdioxidreduktion liegt bei -0,52 V (gegen SCE) bei einem pH-Wert von pH 5,2. Im Versuch mit Pyridin wurde die Kohlenstoffdioxidreduktion schon bei -0,4 V (gegen SCE) mit einem Faraday-Wirkungsgrad von 88 % bis 100 % gemessen. Ohne Pyridin wurde keine Umwandlung gemessen. Die Reaktion war über 30 Stunden stabil und es wurde ein linearer Zusammenhang zwischen der produzierten Methanolmenge und der geflossenen Ladung gefunden. Die Autoren geben die optische Umwandlungseffizienz, also das Verhältnis von optisch eingebrachter Energie zu chemisch gewonnener Energie, mit Werten zwischen 4,8 % und 10,9 % an.
Einen ganz anderen und nicht minder interessanten Weg gehen Autoren der Pennsylvania State University und der Nanjing University of Technology [6]. Sie haben zunächst auf einer Titanoberfläche durch Anodisation in einem Elektrolyten aus Ethylenglykol mit 0,3 Gew.-% Ammoniumfluorid und 3 Vol.-% Wasser bei 55 V Nanoröhrchen aus Titandioxid hergestellt. Nach einer Prozesszeit von sieben Stunden waren Röhrchen mit einem Durchmesser von etwa 70 nm, einer Wandstärke von etwa 20 nm und einer Länge von 30 µm entstanden. Diese wurden anschließend mit deionisiertem Wasser gespült und dann in einem Ofen unter Sauerstoffatmosphäre bei 540 °C für drei Stunden rekristallisiert.
In diesen Nanoröhrchen wurden nun in einem so genannten solvothermischen Prozess Platin-Nanopartikel abgeschieden. Dazu wurde Methanol mit Hexachloroplatinsäure (H2PtCl6) versetzt und die Röhrchen wurden über Nacht in dieser Lösung belassen. Anschließend wurde das Ganze in einer entsprechenden Kammer innerhalb von fünf Minuten auf 120 °C erhitzt und 20 Minuten bei dieser Temperatur gehalten. Anschließend wurden die Röhrchen gut gespült. Abbildung 6 illustriert diesen Prozess. Im Transmissionselektronenmikroskop waren in den Nanoröhrchen die Platinpartikel mit einem Durchmesser zwischen 1,8 nm und 4,9 nm zu sehen. In verschiedenen Versuchen konnte die Partikelgröße durch Variation der Precursorkonzentration verändert werden.
Die so präparierten Titandioxid-Nanoröhrchen wurden in einer beleuchteten Kammer mit Wasserdampf und gasförmigem Kohlendioxid beaufschlagt. Eine Analyse der Gase in der Kammer ergab die Produktion von Methan.
Die bisher beschriebenen Prozesse setzen Kohlenstoffdioxid entweder direkt an der Katalysatoroberfläche oder mit Hilfe eines im Arbeitsmedium befindlichen weiteren Katalysators um. In der Literatur werden aber auch Reaktionen beschrieben, bei denen dem Arbeitsmedium eine Substanz zugegeben wird, die im Lauf der Reaktion Elektronen für die Reduktion des Kohlenstoffdioxids abgibt und damit selbst verbraucht wird. Diese Art der Prozesse ist für die praktische Umsetzung der Technologie nicht sinnvoll und wird daher hier auch nicht weiter betrachtet. Einen guten Überblick über alle aktuell in der Forschung verfolgten Ansätze mit Reaktionsschemata bieten die Reviewartikel von Kumar et al. [1] sowie Yui et al. [3].
5 Einflussfaktoren auf photokatalytische Prozesse
Aus der Literatur lassen sich eine Reihe von Faktoren entnehmen, die ein photokatalytisches System stark beeinflussen. Diese gilt es gleichzeitig zu betrachten und im Hinblick auf eine Zielreaktion möglichst optimal zu wählen. Dazu gehören unter anderem:
- die Größe der Bandlücke des photoaktiven Materials; sie entscheidet darüber, welcher Teil des Spektrums nutzbar ist
- die Lage von Valenz- und Leitungsband; das Energieniveau des Valenzbandes sollte unter dem Potential für die angestrebte chemische Reaktion liegen und das Energieniveau des Leitungsbandes sollte darüber liegen
- die Selektivität des Katalysators für bestimmte Reaktionen, also die entsprechenden Überspannungen
- die Kinetik der Reaktion
Durch Veränderung des Elektrodenmaterials kann die Größe und Lage der Bandlücke angepasst werden. Die Selektivität lässt sich durch geschickte Kombination eines photoaktiven und eines katalytisch aktiven Materials realisieren. Dabei sind stets die Stabilität der gesamten Elektrode und die Empfindlichkeit für eine Katalysatorvergiftung durch Nebenprodukte zu prüfen. Für eine effiziente Umwandlung von Kohlenstoffdioxid in Methanol ist Pyridin als Katalysator vorteilhaft. Zur Langzeitstabilität eines solchen Systems gibt es bisher allerdings keine Untersuchungen. Auch der Einfluss des Herstellverfahrens für die photokatalytischen Werkstoffe ist zu beachten, denn es beeinflusst die Oberflächengestalt der Werkstoffe und damit das Verhalten und die Reaktivität in den chemischen Prozessen.
Bisher wurden viele wissenschaftliche Grundlagen für die Gewinnung von Methanol aus Kohlenstoffdioxid erarbeitet, aber nur wenige Forscher beschäftigen sich mit der praktischen Umsetzung dieser Erkenntnisse. Dies mag unter anderem auch daran liegen, dass die Wirkungsgrade heute im Vergleich mit anderen energieliefernden Prozessen noch eher bescheiden sind. Vielleicht liegt das Augenmerk der meisten Forscher eher auf den Werkstoffen mit der Hoffnung, hier einen Durchbruch zu wesentlich höheren Wirkungsgraden zu erreichen.
6 Anlagentechnik/Zellaufbau
Die oben beschriebenen Reaktionen zur Gewinnung von Methanol aus Kohlenstoffdioxid wurden fast ausschließlich unter Laborbedingungen in sehr kleinem Maßstab betrieben. Aufbauten, die eine Nutzung der Reaktionen in größerem Maßstab erlauben, sind bisher kaum bekannt geworden. Schon 1983 untersuchten Halmann et al. die Möglichkeiten, in einem Solarmodul die Kohlenstoffdioxidreduktion durchzuführen. Verschiedene oxidische Halbleiter wie TiO2, SrTiO3 und CaTiO3 wurden untersucht, die Umwandlungseffizienz der Systeme von Lichtenergie in chemische Energie lag zwischen 0,001 % und 0,016 % [7].
Eine photokatalytische Zelle für die praktische Anwendung muss verschiedene Anforderungen erfüllen:
- Das Kohlenstoffdioxid muss in guten Kontakt mit der Elektrodenoberfläche gebracht werden; in wässrigen Systemen bedeutet das eine möglichst feine Verteilung der Kohlenstoffdioxid-Gasblasen
- Die effiziente Abfuhr des Produktes aus der Zelle ist wichtig, um die chemischen Reaktionen zu erleichtern. Eine hohe Produktkonzentration in der Zelle würde zu einer Verringerung der Reaktionsgeschwindigkeit bei der Bildung des Produktes führen. Dabei darf Kohlenstoffdioxid aber nicht aus dem Arbeitsmedium der Zelle entfernt werden
- Falls der Katalysator aus Partikeln besteht, die im Arbeitsmedium zirkulieren, muss die Konstruktion der Zelle sicherstellen, dass alle Partikel regelmäßig von Licht bestrahlt werden und der Transport von Kohlenstoffdioxid zur Partikeloberfläche keinen Engpass für die chemischen Reaktionen darstellt
- Der Energieaufwand für den Transport aller Medien sollte so gering wie möglich sein; ideal wäre eine Nutzung der Lichtenergie auch dafür
- Die Zelle sollte einfach aufgebaut und zerlegbar sein, damit eine Reparatur möglich ist. Zudem dürfen nur solche Materialien eingesetzt werden, die möglichst leicht und gleichzeitig über lange Zeit stabil in Sonnenstrahlung sind
- Auch das Arbeitsmedium in der Zelle muss über lange Zeit stabil sein und darf seine Eigenschaften hinsichtlich der chemischen Reaktionen nicht verändern
- Falls ein Katalysator eingesetzt wird, darf sich dieser über die Zeit nicht zersetzen oder Abbauprodukte bilden, die schädlich für die Bildung des Produktes sind
In Abbildung 7 ist eine Zelle schematisch abgebildet, in der Partikel aus Lichtsammler und Katalysator im Arbeitsmedium suspendiert sind. Die gleichmäßige Vermischung der Partikel und des Kohlenstoffdioxids sowie die anschließende Trennung von Medium, Partikeln und Kohlenstoffdioxid einerseits und Methanol andererseits ist hier die verfahrenstechnische Herausforderung. Generell ist je nach technischem Konzept und Form des Katalysators die Systemtechnik zum Betrieb einer solchen photokatalytischen Reaktionszelle komplex und erfordert einige Forschungsarbeiten.
Geeignete Zellen für die praktische Herstellung solarer Energieträger in größerem Maßstab wurden bisher in der Literatur nicht beschrieben. Der Schwerpunkt der Forschungen liegt entweder in der Aufklärung von Reaktionen oder in ihrer Optimierung hinsichtlich des Wirkungsgrades bei der Nutzung der Lichtenergie. Die für eine praktische Anwendung relevanten Fragestellungen wurden bisher aber noch kaum bearbeitet. Für eine breitere Nutzung wären großflächige Zellen ähnlich den Photovoltaikmodulen notwendig, die einfach auf größeren Flächen aufgebaut und betrieben werden könnten. Zusätzlich wird für den Betrieb eine Infrastruktur aus Kohlenstoffdioxidgewinnung und Produktabtrennung und Reinigung benötigt, deren technische Grundkonzepte noch erarbeitet werden müssen. Ohne Testplattformen sind auch die weiteren Optimierungen der Katalysatorsysteme nur begrenzt sinnvoll, denn für den praktischen Einsatz ist Systemwissen über das Zusammenspiel aller Komponenten erforderlich, das sich in Teilen nur empirisch gewinnen lässt.
Auch auf europäischer Ebene gab und gibt es Forschungsaktivitäten zum Thema der solaren photokatalytischen Prozesse. Von 2009 bis Ende 2011 wurden im Projekt NANOPEC verschiedene oxidische Halbleiter und Elektroden entwickelt, um eine optimierte photokatalytische Herstellung von Wasserstoff zu realisieren. Neben der Polytechnischen Hochschule Lausanne (EPFL) waren sieben weitere Forschungspartner daran beteiligt. Auch in dem seit Anfang 2013 laufenden Projekt Solarogenix sollen nanostrukturierte Photokatalysatoren aus Oxiden entwickelt werden. Hier ist ebenfalls die Produktion von Wasserstoff das Ziel, allerdings soll er aus Salzwasser gewonnen werden. Durch das Verständnis der beteiligten physikalischen und chemischen Mechanismen auf atomarer Ebene soll die Entwicklung effizienter Katalysatoren möglich werden. Die Ergebnisse sollen mit Hilfe von Industriepartnern in Demonstratoren umgesetzt werden. Diese Module werden dann zum Test der Werkstoffe unter realen Bedingungen verwendet.
Die Erzeugung solarer Energieträger wie Wasserstoff, Methan oder Methanol ist eine sinnvolle Nutzung von solarer Energie, denn unsere Gesellschaft ist fast vollständig auf die Nutzung von chemisch gebundener Energie ausgerichtet. Unsere gesamte Infrastruktur, unser Alltag und unsere Lebensweise basieren darauf. Wenn es also gelänge, mit Hilfe von solarer Energie zumindest einen Teil der heute genutzten fossilen chemischen Energieträger durch solar erzeugte Energieträger zu ersetzen, dann könnten wir die Energiewende noch wirkungsvoller gestalten.
Literatur
[1] Kumar, B.; Llorente, M.; Froehlich, J.; Dang, T.; Sathrum, A.; Kubiak, Clifford: Photochemical and photoelectrochemical Reduction of CO2; Annual Review of Physical Chemistry, 63 (2012), S. 541–569
[2] Joshi, U.; Palasyuk, A.; Arney, D.; Maggard, Paul: Semiconducting oxides to facilitate the conversion of solar energy to chemical fuels; The Journal of Physical Chemistry Letters (2010)1, S. 2719–2726
[3] Yui, T.; Tamaki, Y.; Sekizawa, K.; Ishitani, O.: Photocatalytic Reduction of CO2: From Molecules to Semiconductors; Top Curr Chem (2011)303, S. 151–184
[4] Yuan, J.; Hao, C.: Solar-driven phtotoelectrochemical reduction of carbon dioxide to methanol at CuInS2 thin film photocathode; Solar Energy Materials and Solar Cells, 108 (2013), S. 170–174
[5] Barton, E.; Rampulla, D. M.; Bocarsly, A. B.: Selective Solar-driven reduction of CO2 to methanol using a catalyzed p-GaP based photoelectrochemical cell; Journal of the American Chemical Society, 130 (2008), S. 6342–6344
[6] Feng, X.; Sloppy, J. D.; LaTempa, T. J.; Paulose, M.; Komarneni, S.; Bao, N.; Grimes, C. A: Synthesis and deposition of ultrafine Pt nanoparticles within high aspect ratio TiO2 nanotube arrays: application to the photocatalytic reduction of carbon dioxide; Journal of Materials Chemistry, 21 (2011), S. 13429–13433
[7] Halmann, M.; Aurian-Blajeni, B.: Photoelectrochemical reduction of carbon dioxide in aqueous solutions on p-GaP electrodes: an a. c. impedance study with phase-sensitive detection; Journal of Electroanalytical Chemistry, (1996)402, S. 97–105
DOI: 10.7395/2013/Brunel