Schichtbildung auf der Elektrode
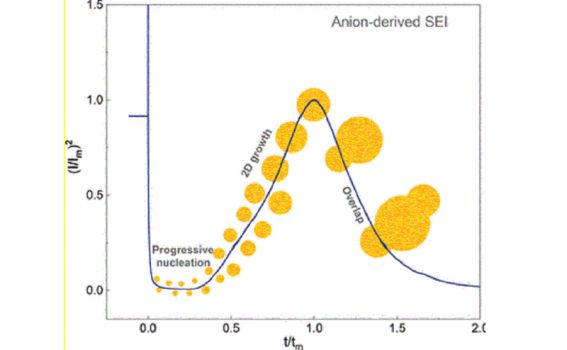
Akkus werden geladen und entladen – alles dank eines perfekten Zusammenspiels von Elektrodenmaterial und Elektrolyt, sollte man meinen. Ohne eine gute Passivierungsschicht geht aber nichts. Materialwissenschaftler haben nun einen atomaren Blick auf die Entstehung der Schicht auf der Elektrode geworfen. Wie sie in ihrer Studie in der Zeitschrift Angewandte Chemie erläutern, sollten hierfür Lithiumsalz und Lösungsmittelmoleküle im Elektrolyten gut aufeinander abgestimmt sein.
In Lithium-Ionen-Batterien bildet sich die Passivierungsschicht beim ersten Anlegen einer Spannung. Bestandteile aus dem Elektrolyten lagern sich auf der Graphitelektrode ab und bilden einen Überzug, der rasch die gesamte Elektrode bedeckt. Erst nach Fertigstellung dieser Schicht können sich die positiven Lithium-Ionen in die Elektrode für das Aufladen einlagern, ohne dass das Elektrodenmaterial abblättert.
Qiang Zhang von der Tsinghua-Universität in Beijing und Kollegen haben nun die genauen Vorgänge bei der Keimbildung und der Ausbreitung der Passivierungsschicht untersucht. In Lithium-Ionen-Akkus enthält der Elektrolyt das Lithiumsalz mit einem Lösungsmittel. Starke Lösungsmittel hüllen das positive Lithium-Ion des Lithiumsalzes vollständig ein, während die negativ geladenen Anionen sich frei bewegen können. Bei schwächeren Lösungsmitteln bleiben die Anionen näher am Lithium-Ion und sind Bestandteil der inneren Solvathülle.
Diese innere Solvathülle muss das Lithium-Ion an der Elektrode abstreifen, damit die Passivierungsschicht entsteht. Die Forscher konnten zeigen, dass beim Anlegen einer Spannung an der frischen Graphitelektrode sich zuerst die negativen Ionen aus der inneren Hülle auf der Oberfläche ablagern. Anschließend nehmen sie in einer elektrochemischen Reaktion zwei Elektronen von der Elektrode auf. Die somit reduzierten Anionen zersetzten sich und bildeten die Keime für die Kristallisation der Passivierungsschicht. Das bedeutet, schlussfolgern die Autoren, dass sich eine gute kristalline Passivierungsschicht ausbildet, wenn die Anionen leichter als die Lösungsmittelmoleküle Elektronen aufnehmen und sich zersetzen.
Die Wissenschaftler untersuchten nun mit elektrochemischen Techniken und Rasterkraftmikroskopie das weitere Kristallwachstum bis zur Ausbildung einer vollständigen Deckschicht. Sie stellten fest, dass sich eine gleichmäßige Schicht nur bei geringen Überspannungen bildete. Das Lösungsmittel beeinflusste die Überspannung: Bei Lösungsmitteln, die die Kristallschicht gut benetzten, stellte sich gar keine Überspannung ein.
Daraus schlossen die Autoren, dass bei der Entwicklung von leistungsfähigen Elektroden mehr auf das Zusammenspiel zwischen den negativen Ionen des Lithiumsalzes und dem Lösungsmittel geachtet werden sollte. Damit sich eine gleichmäßige anorganische Schicht bildet, sollten sich die negativen Ionen des Lithiumsalzes gut auf der Elektrodenoberfläche ablagern können und leichter elektrochemische Reaktionen eingehen als die Lösungsmittelmoleküle. Die festen Zersetzungsprodukte sollten nicht löslich sein, sich aber dennoch gut mit dem Lösungsmittel verbinden.
Autor: Qiang Zhang, Tsinghua University (China),
Originalpublikation: https://doi.org/10.1002/ange.202100494
Aktuelle Onlineartikel
-

09. 04. 2024 Entsorgungslogistik von Elektro-Altgeräten ganz neu gedacht
-

09. 04. 2024 Fertigungstechnologien für die Zukunft der europäischen Raumfahrt
-

08. 04. 2024 Druck- und Temperaturmessung im Wälzkontakt unter Mischreibung dank innovativem Dünnschicht-Multisensor
-
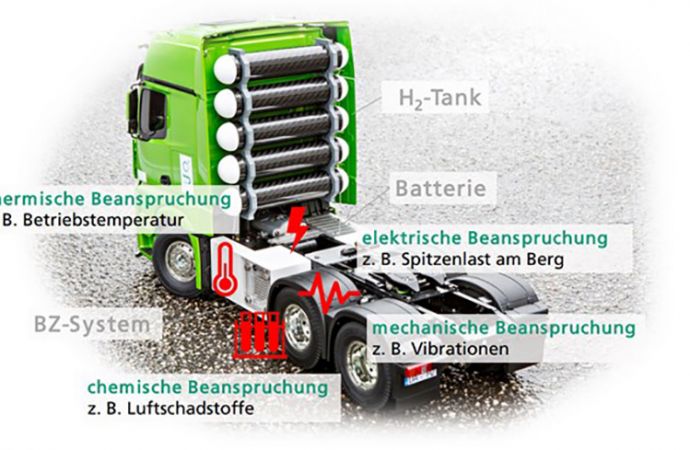
05. 04. 2024 Brennstoffzellensysteme unter Vibrationslasten testen und verstehen
-

14. 03. 2024 Forschen im Pop-Up-Labor: CAIS erhält € 170.000 für transdisziplinäres Forschungsprojekt
-

13. 03. 2024 Grüne Startups als treibende Kräfte für eine nachhaltige Wirtschaft